 |
21일 한국거래소에 따르면 유한양행은 오후 2시22분 현재 전 거래일 대비 2.77%(2600원) 오른 9만6700원에 거래되고 있다. 또한 유한양행우는 27.72%(2만1900원) 오른 10만900원에 거래되고 있다. 우선주는 장중 상한가(10만2700원)을 터치하기도 했다.
이는 폐암 신약 렉라자가 미국 FDA 승인을 받은 사실에 긍정적인 투심이 매수세에 훈풍을 불어넣는 것으로 보인다.
유한양행이 폐암 치료제로 개발한 국산 31호 신약 ‘렉라자’가 미국에서 병용요법으로 품목허가를 받았다. 바이오시밀러가 아닌 국산 항암제 신약이 미국에서 허가를 받은 것은 이번이 처음이다.
유한양행은 20일 미국 식품의약국(FDA)이 3세대 폐암 신약 ‘렉라자(성분명 레이저티닙 메실산염일수화물, 미국 제품명 라즈클루즈)’와 미국 제약사 존슨앤드존슨(J&J)의 표적이중항체(EGFR·c-MET) 폐암 치료제 ‘리브리반트(아미반타맙)’의 병용요법에 대한 1차 치료제 사용을 승인했다고 밝혔다.
렉라자와 리브리반트 병용요법을 상피세포성장인자수용체(EGFR, Epidermal Growth Factor Receptor) 엑손19 결실 또는 엑손21(L858R) 치환 변이가 확인된 국소 진행성 또는 전이성 비소세포폐암(NSCLC) 성인 환자의 초기 치료제로 사용할 수 있게 된 것이다.
렉라자는 EGFR 돌연변이 양성 비소세포폐암 치료제로 개발된 3세대 항암제 신약이다. 국내 제약사 오스코텍 자회사(제노스코)가 레이저티닙을 개발했고 전임상 단계에서 유한양행에 기술을 이전해 렉라자로 완성됐다.
국내에서는 EGFR 돌연변이(엑손19 결실·엑손21 치환 변이) 국소 진행성 또는 전이성 비소세포폐암 환자 치료를 위한 단독요법 1차 치료제로 사용되고 있다. 급여 처방(1~2차 치료)도 가능하다.
폐암은 전 세계적으로 환자 수가 많고 사망률이 높은 질환으로 가장 큰 항암제 시장을 형성하고 있다. 작년 기준 글로벌 시장 규모는 약 46조 원에 달하는 것으로 알려졌다.
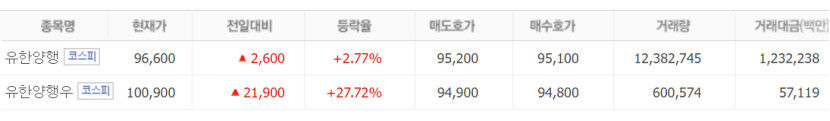 |
| 출처:네이버 pay 증권 |
지난 2021년 1월 국산 신약으로 허가 받은 렉라자는 작년 6월 국내 1차 치료제로 허가가 확대된 이후 6개월 만에 건강보험 급여가 적용됐다. 올해 1분기 200억 원대 처방 실적을 기록했고 연내 1000억 원 돌파를 예상하고 있다. 또한 이번 병용요법 허가가 유럽과 중국, 일본 등 다른 국가 승인심사와 국내 처방 확대에 긍정적인 영향을 줄 것으로 기대하고 있다.
서용덕기자

서용덕
영남일보(www.yeongnam.com), 무단전재 및 수집, 재배포금지

![[영상] 김부겸·추경호 나란히 출사표…6·3 지방선거 대구 시장 후보 등록 시작](https://www.yeongnam.com/mnt/webdata/content/202605/5_ㅇㄹㄴㄹㄴㅇㄹㄴㅇㄹ.png)


